Marcel Dion und Wayne Parker
Grundprinzipien der Dampfsterilisation
In diesem Artikel wird das Grundprinzip der Dampfsterilisation erläutert, womit durch ein solides Verständnis des Verfahrens die häufigsten Fehler bei der Verwendung von Autoklaven vermieden werden sollen.
Die Dampfsterilisation ist ein Verfahren das seit mehr als einhundert Jahren zur Sterilisierung von feuchtigkeits- und hitzebeständigen Produkten verwendet wird. Dabei wird Wasser in Dampf umgewandelt, der nicht toxisch, in der Regel jederzeit verfügbar ist und sich relativ einfach handhaben lässt. Ein solides Verständnis des Grundprinzips der Dampfsterilisation und der dabei ablaufenden Zyklen ist erforderlich, um Fehler zu vermeiden, in deren Folge Ladungsteile nicht sterilisiert werden, die Funktion der Ausrüstung unzureichend ist oder sich Verletzungen des Bedienpersonals, verminderte Produktivität, erhöhte Betriebs- und Wartungskosten sowie Beschädigungen von Ladungsteilen ergeben. Dampfsterilisatoren werden für zahlreiche Anwendungen in der Pharmazie und Medizintechnik eingesetzt. In diesem Artikel wird vorrangig auf Anwendungen mit gesättigtem Dampf eingegangen, wie der Sterilisation von Labormaterialien, Dekontamination und Sterilisation allgemeiner Komponenten. Zur abschließenden Sterilisation von parenteral zu verabreichenden Flüssigkeiten oder von Geräten mit Flüssigkeiten sind ggf. Verfahren mit einem Dampf-Luft-Gemisch oder überhitztem Wasser-Luft-Gemisch erforderlich. Diese Verfahren sowie die In-situ-Sterilisation von Speicherbehältern, Filtern usw. werden in diesem Artikel nicht beschrieben.
Grundprinzipien der Dampfsterilisation
Für eine erfolgreiche Dampfsterilisation sind sechs Faktoren von entscheidender Bedeutung:
1. Zeit
2. Temperatur
3. Feuchtigkeit
4. Direkte Dampfeinwirkung
5. Entlüftung
6. Trocknung
1. Zeit
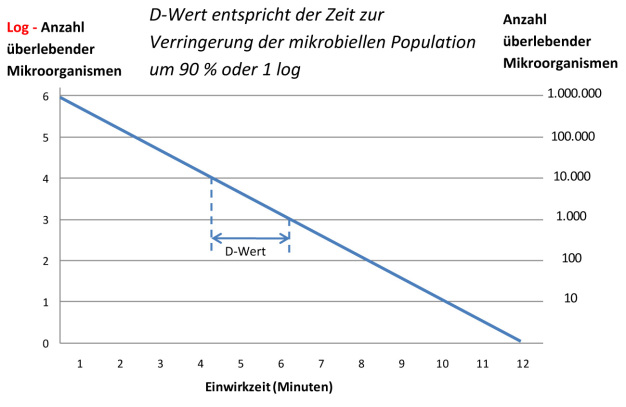
Die Einwirkzeit (Sterilisation) ist ein kritischer Faktor, da nicht alle Organismen in einem einheitlichen Zeitintervall abgetötet werden. Daher ist die Sterilisationstemperatur über eine Mindestzeitdauer zu halten, um alle Organismen abzutöten. Zur Prüfung der Zyklen von Dampfsterilisiergeräten werden gängigerweise Geobacillus stearothermophilus (Bst)-Sporen verwendet, da diese extrem resistent gegenüber der Sterilisation mit feuchter Hitze sind. Sie sind außerdem nicht pathogen und jederzeit gewerblich erhältlich. Die Anzahl überlebender Sporen wird i. d. R. auf einer logarithmischen Skala dargestellt. Bei dieser Darstellung ergibt sich typischerweise – wie in Abbildung 1 – ein linearer Verlauf der überlebenden Sporen im Verlauf der Zeit.
Der D-Wert (Zeit zur Reduzierung der mikrobiellen Population um 90 %) für Bst muss 1,5 bis 3,0 Minuten bei 121,1 °C (250 °F) (1) liegen. Für die Darstellung in diesem Artikel wird ein D121 -Wert von 2,0 Minuten und eine Sterilisationstemperatur von 121 °C (250 °F) verwendet. Ein typischer Sterilisationszyklus umfasst bei einer angenommenen Anfangspopulation von einer Million (106) Organismen eine Einwirkphase von mindestens 20 Minuten bei einer Temperatur von 121 °C (250 °F), um einen SAL (Sterility Assurance Level) von 10-4 zu erreichen. Das bedeutet, dass nach dem Verfahren eine Wahrscheinlichkeit von einer von zehntausend (10-4) überlebenden Bst-Spore besteht. Der SAL verringert sich mit jeder 2-minütigen Verlängerung der Einwirkzeit bei 121 °C (250 °F) um den Faktor 10. Der erforderliche SAL variiert je nach Anwendung. Vor der Zyklusentwicklung muss darauf geachtet werden, dass der korrekte SAL angestrebt wird. Die tatsächlichen Keime des Sterilisierguts werden natürlich schneller als die Bst-Sporen abgetötet. Die sich daraus ergebende Unverhältnismäßigkeit ist bei der Sterilisation von haltbaren Produkten gängige Praxis und sollte wenn möglich angewendet werden(2).
2. Temperatur
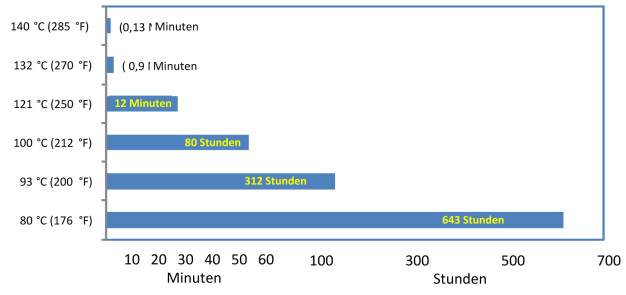
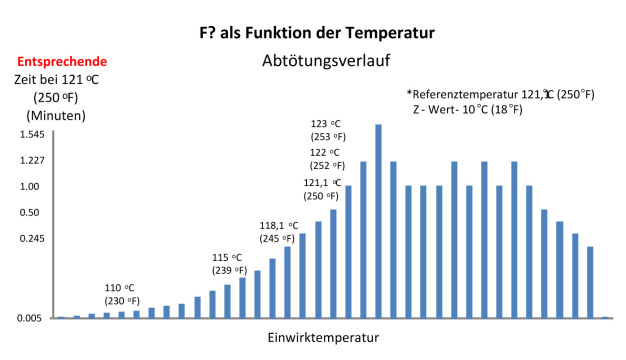
Der zweite kritische Faktor bei der Dampfsterilisation ist die Temperatur des gesättigten und in der Sterilisatorkammer kontrollierten Dampfes. In Abbildung 2 unten wird deutlich, wie durch Anstieg der Temperatur sich die für die Sterilisation notwendige Zeit drastisch verkürzt. Abbildung 2 zeigt grob wie viel Zeit notwendig ist, um eine äquivalente Abtötung von Mikroorganismen (SAL 100 bei einer Anfangspopulation von 106, D121-Wert: 2,0 Minuten) bei unterschiedlichen Einwirktemperaturen der feuchten Hitze(2) zu erzielen. Die Temperatur des gesättigten Wasserdampfs hängt direkt mit dem Druck zusammen, der auf den Dampf einwirkt. Die Werte für die Druck-Temperatur-Korrelation werden in Tabellen für gesättigten Dampf dargestellt(4). Bei einem typischen Zyklus bei einer Temperatur von 121 °C (250 °F) ist in der Sterilisatorkammer ein Druck von 103 bis 117 kPa notwendig. Der gemessene Druck wird aufgrund des enthaltenen Luftgemischs und der geografischen Höhe über dem Meeresspiegel größer als der Druck laut Tabellenwert sein. Der maximale Druck in einem Autoklav ist in der Spezifikation (ASME (American Society of Mechanical Engineers)-Druckangaben) des Druckbehälters (Kammer und Mantel) angegeben und darf nicht überschritten werden.
3. Feuchtigkeit
Der Feuchtigkeitsgehalt im Dampf wirkt sich wesentlich auf dessen Denaturierungs- bzw. Eiweißgerinnungsfähigkeit aus. Daher ist es wichtig, dass gesättigter Dampf verwendet wird. Gesättigter Dampf bildet mit erhitztem Wasser bei gleichem Druck ein Gleichgewicht, d. h. der Dampf enthält den höchsten Feuchtigkeitsanteil bevor sich flüssiges Kondensat bildet. Zur Dampfsterilisation wird gesättigter Dampf empfohlen. In Sterilisiergeräten sind nicht alle Arten von Dampf zulässig. Es wird eine getrennte Reindampfzufuhr empfohlen. Zu vermeiden sind überhitzter Dampf, Dampf mit übermäßigem flüssigen Wasseranteil und Dampf mit Kessel- oder Siedezusätzen oder Verunreinigungen (z. B. Rost). Überhitzter Dampf ist Dampf oberhalb der Sättigungstemperatur. Zu Überhitzung kommt es in Dampfverteilern, wenn der Leitungsdruck über das Druckminderventil abfällt. Je größer der Druckabfall, desto mehr Überhitzung wird erzeugt. Überhitzter Dampf enthält nicht die erforderliche Feuchtigkeit, um eine sichere Sterilisation zu gewährleisten. Die im überhitzten Dampf enthaltene überschüssige Energie verflüchtigt sich und wird letztlich vom Sterilgut in der Sterilisationskammer an die Umgebung abgegeben. Sie kann jedoch bei der Validierung des Sterilisiergeräts gemäß der Anforderungen zur Temperaturstabilisierung in der leeren Kammer nach EU-Norm EN 285(5) problematisch sein. Das ideale Reindampfsystem für Dampfsterilisatoren wird auf 207 bis 241 kPa an der Einspeisung eingestellt. Nach EN 285 darf der Druck der Dampfzufuhr nicht höher als der doppelte Kammerdruck bei gewünschter Temperatur sein. Zur Überhitzung kommt es auch dann, wenn gesättigter Dampf über eine Oberfläche mit höherer Temperatur geführt wird. Die Temperatur im Mantel des Sterilisiergeräts muss stets leicht unter der Sterilisationstemperatur in der Kammer liegen, um eine Überhitzung des in die Kammer einströmenden Dampfs zu vermeiden.
4. Direkte Dampfeinwirkung
Damit die im Dampf gespeicherte Energie auf das Sterilisiergut übertragen werden kann, müssen diese einer direkten Dampfeinwirkung ausgesetzt werden. Ohne direkte Dampfeinwirkung auf alle Oberflächen wird das Sterilisiergut nicht umfassend sterilisiert. Die Energiespeicherkapazität von Dampf ist bei gleicher Temperatur wesentlich größer als die von trockener Luft oder Wasser. Aus der oben genannten Tabelle für gesättigten Dampf lässt sich entnehmen, dass für die Erwärmung von Wasser von 0 °C auf 100 °C (32 °F auf 212 °F) 419 kJ/kg notwendig sind. Das bezeichnet man als die Enthalpie von Wasser (hl). Zur Erzeugung von Dampf bei atmosphärischem Druck (100 °C oder 212 °F) werden weitere 2.257 kJ/kg benötigt. Diese zusätzlich im Dampf gespeicherte Energie bezeichnet man als die Verdampfungsenthalpie (he), sie fungiert als Kernprinzip der Dampfsterilisation. Um die im Dampf gespeicherte Energie abzugeben, muss sie auf den Oberflächen des Sterilisierguts kondensieren.
5. Entlüftung
Luft ist bei der Dampfsterilisation der größte Störfaktor. Daher muss Luft aus der Sterilisierkammer und der Ladung entfernt werden, bevor die Dampfeinwirkzeit und die Sterilisation erfolgen können. Das wird in Dampfsterilisatoren vor der Sterilisation (Vorkonditionierungsphase) durch eine Reihe von Vakuumimpulsen erreicht. In der Autoklavkammer wird immer ein geringer Luftanteil vorhanden sein, der jedoch auf ein Minimum begrenzt werden muss. Die häufigsten Ursachen für eine unzureichende Sterilisation sind eine ungenügende Entlüftung, Leckagen des Kammervakuums und minderwertige Dampfqualität (Übermaß an nicht kondensierbaren Gasen).
6. Trocknung
Verpackte Sterilgüter müssen trocken sein, bevor sie aus dem Sterilisator aseptisch entnommen werden können. Kondensation ist der natürliche Vorgang, bei dem Dampf mit kühleren Oberflächen der Ladung während der Aufheiz- und Einwirkphasen in Berührung kommt. Durch Kondensation (feuchte Verpackungen oder Beutel) kann es bei der Entnahme aus dem Sterilisiergerät zu einer erneuten Kontamination der Ladung kommen. Im Dampfsterilisator wird die Ladung nach erfolgter Sterilisation durch Erzeugung eines Feinvakuums in der Sterilisierkammer (Nachkonditionierungsphase) getrocknet. Für eine effiziente Trocknung wird eine Vakuumqualität von 6,9 bis 13,8 kPa empfohlen. Bei einem Druck von 6,9 kPa in der Sterilisierkammer siedet Wasser bereits bei 38,7 °C (101,7 °F). Das Kondensat verdampft und der Dampf wird über das Vakuumsystem des Sterilisators entfernt. Die zum Verdampfen des Kondensats notwendige Energie wird vom Sterilgut selbst geliefert. Während die Temperatur des Sterilguts aufgrund der Verdampfung des Kondensats sinkt, verringert sich die Verdampfung (Trocknung). Ist der Siedepunkt des Wassers bei Vakuumtrocknung erreicht, ist die Trocknung vernachlässigbar. Wird die Zeit zur Trocknung über diesen Punkt hinaus erhöht, ergibt sich dadurch kein zusätzlicher Trocknungseffekt. Die optimale Trocknungszeit des Sterilguts ergibt sich hauptsächlich aus der Ladungsdichte und der Verpackung. Plastik- und Gummiteile erfordern ggf. aufgrund ihrer geringeren Dichte eine zusätzliche Trocknung, da sie schnell abkühlen (Nachkonditionierungsverfahren mit gepulster Luft- oder erwärmter gepulster Lufttrocknung). Die Menge an Restfeuchtigkeit in einer Verpackung lässt sich durch Abwiegen der Verpackung vor und nach dem Sterilisationsverfahren bestimmen. In der Regel ist jedoch eine Prüfung auf nicht vorhandene Wassertropfen an oder in der Verpackung ausreichend.
Grundlegende Zyklen der Dampfsterilisation
Die Zyklen der Dampfsterilisation bestehen aus den folgenden drei Phasen:
1. Vorkonditionierung: Während dieser Phase wird Luft aus der Sterilisierkammer entfernt und das Sterilisiergut wird durch abwechselnde Vakuum- und Druckpulse befeuchtet.
2. Einwirkzeit: In dieser Phase wird die Temperatur der Sterilisierkammer erhöht und für die Dauer der programmierten Einwirkzeit auf festgelegter Sterilisationstemperatur gehalten (beide sind vom Benutzer einstellbar). Die Einwirkzeit kann auch durch die akkumulierte Fo für Flüssigkeiten reguliert werden, wenn eine Chargensonde und angemessene Bedienelemente am Sterilisiergerät verwendet werden. Weitere Informationen zu Fo finden Sie auch unter Punkt #7 im Abschnitt ‚Häufige Fehler‘.
3. Nachkonditionierung: In dieser Phase wird das trockene Sterilstückgut oder flüssiges Gut gekühlt und ggf. getrocknet. Der Druck der Sterilisierkammer wird auf atmosphärisches Niveau geführt.
Für unterschiedliche Anwendungen wurden über die Jahre verschiedene Zyklen entwickelt. Die Verwendung der entsprechenden Zyklen ist entscheidend.
- Für Sterilisiergut, wie unverpackte Metallteile, Glas oder nicht poröses Material, die keine Luft einschließen, kann ein Basis-Gravitationszyklus (Zyklus ohne Vorvakuum) zur Anwendung kommen.
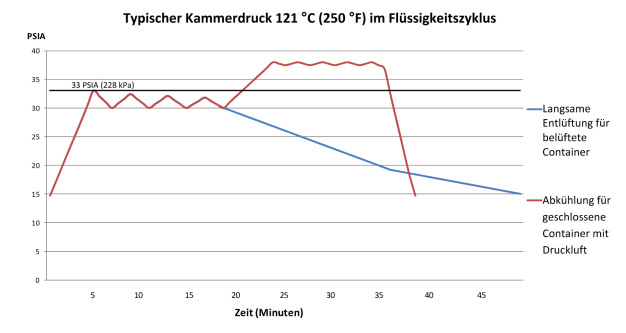
- Für Flüssigkeiten sind modifizierte Gravitationszyklen notwendig, um Flüssigkeitsverluste durch ein Überkochen zu vermeiden. Flüssigkeiten in offenen oder belüfteten Containern oder in Flaschen mit losen Verschlüssen lassen sich in einem „Basis“-Flüssigkeitszyklus (mit langsamer Entlüftung) verarbeiten. Während der Abkühlphase (Entlüftung) dieses Zyklus wird der Druck in der Sterilisierkammer langsam auf ein atmosphärisches Niveau abgesenkt, um ein Überkochen – wie in Abbildung 3 gezeigt – zu verhindern. Der nominale Flüssigkeitsverlust durch Verdampfung während der langsamen Entlüftungsphase liegt typischerweise bei 10 bis 15 %. Die für die langsame Entlüftung notwendige Zeit kann je nach Flüssigkeitsvolumen pro Container oder pro Ladung variieren. Größere Volumen erfordern langsame Entlüftungsraten. Es empfiehlt sich die Verwendung einer Chargensonde und Messung der F0-Einwirkung. Für dieses Verfahren sind ausschließlich belüftete Container zu verwenden.
Die Temperatur der Flüssigkeiten nach dem langsamen Entlüftungszyklus liegt etwa am Siedepunkt. Vor der Entnahme aus dem Sterilisiergerät müssen sie deshalb abkühlen. Für Flüssigkeiten in versiegelten Containern ist ein Abkühlzyklus mit Druckluft erforderlich, um eine Explosion des/der Container(s) in der Abkühlphase oder während des Entladevorgangs – wie in Abbildung 3 dargestellt – zu verhindern. Zum Abschluss der Einwirkphase wird saubere, trockene Druckluft (Prozessluft) in die Sterilisierkammer geleitet und mit einem über dem Druck des gesättigten Dampfes liegenden Druckniveau bei Temperatur der Chargensonde gesteuert. Während die Luft über das Sterilgut geleitet wird, kühlt das Sterilgut ab, der Dampf in der Sterilisierkammer kondensiert und der Kammerdruck beginnt zu sinken. Der zugeführte Druckluftstrom muss zur Aufrechterhaltung des Überdrucks während der gesamten Abkühlphase ausreichen. Diese Luftkühlung wird nachdrücklich zur Sterilisation von Flüssigkeiten in versiegelten ODER belüfteten Containern empfohlen, da dadurch während der Abkühlphase keine Verdampfung oder ein Überkochen auftritt. Flüssigkeiten können darüber hinaus während der Phase auf eine Temperatur zur sicheren Handhabung abgekühlt werden (60 °C bis 80 °C oder 140 °F bis 176 °F), indem in der Abkühlphase durch den Mantel des Sterilisators Wasser geleitet wird. Danach lässt sich das Sterilgut sofort nach abgeschlossenem Zyklus entnehmen. Anhand der Druckangaben der American Society of Mechanical Engineers (ASME) zum Sterilisator wird der zulässige Überdruck begrenzt. Das Füllvolumen hat einen signifikanten Einfluss auf den Innendruck des geschlossenen Containers. Je geringer das Füllvolumen, desto niedriger ist aufgrund des Luftdrucks im oberen Containerbereich der Innendruck. Der ungefähre Innendruck eines geschlossenen Containers lässt sich anhand der Robert-Beck-Gleichung (6) errechnen.
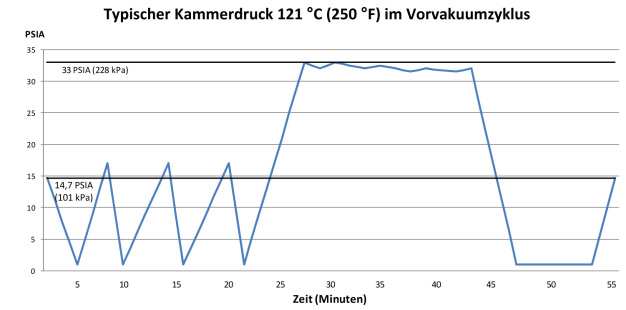
- Für Sterilisiergut außer Flüssigkeiten wird ein „Vorvakuum“-Zyklus (alternierende Vakuum- und Druckvorkonditionierungspulse) empfohlen.
(Abbildung 4)
Ermitteln der Leistungsindikatoren
Die Wirksamkeit des Sterilisationsverfahrens kann anhand verschiedener Methoden überprüft werden. Typischerweise werden Methoden mit biologischen Indikatoren (BIs) und chemischen Indikatoren (CIs) verwendet, die an ungünstigsten (worst case) Positionen der Ladung und/oder in Testpackungen eingesetzt werden.
- Biologische Indikatoren bieten die bestmögliche Sterilisationsprüfung und werden zur Ermittlung der Wirksamkeit des Zyklus herangezogen. In dieser Kategorie sind verfügbar:
> Mit Sporen beimpfte Teststreifen. Diese Streifen müssen kurz nach abgeschlossenem Sterilisationsvorgang in aseptischer Form in ein zu inkubierendes Nährmedium gebracht werden.
> Selbstentwickelnde biologische Indikatoren (SCBI) (Abb. 5) SCBIs sind in sich abgeschlossen, wodurch sich die Wahrscheinlichkeit von verfälschten Positivbefunden aufgrund unzureichend aseptischer Übertragungsverfahren verringert. Mit ihrer Hilfe wird typischerweise die Wirksamkeit des Dampfsterilisationsverfahrens überwacht.
> Wenn Indikatoren in flüssiges Sterilisiergut (z. B. Nährmedium)eingebracht werden müssen, werden auch Glasampullen verwendet.
- Chemische Indikatoren gewährleisten einen unverzüglichen Nachweis des Dampfdurchlasses (nicht notwendigerweise der Sterilisation). In dieser Kategorie sind verfügbar:
> Autoklavstreifen, mit denen nachgewiesen wird, dass der Prozess stattgefunden hat, jedoch ohne Korrelation zu Zeit/Temperatur.
> Chemische Integratoren mit einer Zeit- und Temperaturkorrelation. Mithilfe dieser konkreten Indikatoren lässt sich die Zyklusentwicklungszeit wesentlich durch eine sofortige Indikation der Wirksamkeit des Sterilisationsprozesses reduzieren.
- Untersuchungen des Dampfdurchlasses: An schwer zugänglichen Stellen lassen sich zur Überprüfung des Dampfdurchlasses Temperatursensoren anbringen.
Vorvakuumsterilisatoren müssen routinemäßig auf undichte Stellen und ihre Entlüftungskapazität überprüft werden. Mit der Software für moderne Vorvakuumsterilisatoren werden meist automatische Lecktests (Test der Vakuumhaltedauer) für die Kammer mitgeliefert und diese müssen nach dem Aufwärmzyklus täglich ausgeführt werden. Die Sterilisierkammer wird auf das maximal mögliche Maß des Vakuumsystems evakuiert (< 6,9 kPa) und Kammer und zugehörige Schläuche werden über eine Haltezeitdauer abgetrennt (Ventile werden geschlossen). Die Differenz zwischen dem absoluten Druck am Anfang des Haltezeitraums zu dem absoluten Druck am Ende des Haltezeitraums entspricht der Gesamtleckrate. Die Leckrate sollte < 1,0 mm Hg/min (2) betragen. Der Haltezeitraum schwankt je nach Verfahren zwischen 10 und 30 Minuten. Zu beachten ist, dass ein Druckanstieg im Haltezeitraum nicht zwingend auf eine Vakuumleckage in der Sterilisierkammer hinweist. Durch feuchten Dampf kann während der Testdruckpulse der Vorkonditionierung Kondensat in die Sterilisierkammer eindringen. In der Kammer enthaltenes Kondensat verdampft im Testvakuum und verursacht einen Druckanstieg in der Sterilisierkammer. Zur Ermittlung der Ursache des Druckanstiegs kann z. B. die Leckrate während der Vakuumhaltedauer mit einem an der Sterilisierkammer angeschlossenen absoluten Druckmessgerät überwacht werden. Eine Luftleckrate wird über die Vakuumhaltedauer relativ konstant sein. Ein Druckanstieg, der aus der Verdampfung von Kondensat herrührt, wird sich als anfänglich hoher Wert darstellen, der mit der Verdampfung abfällt.
Zusätzlich zum Vakuumhaltetest sollte ein Test mit einer Versuchsladung, wie z. B. der Bowie-Dick-Test in Abbildung 6, regelmäßig durchgeführt werden. Der Test mit einer Versuchsladung unterscheidet sich vom Vakuumhaltetest dadurch, dass dabei die Luft aus einer kompakten Verpackung vom Sterilisator entfernt und durch Dampf ersetzt werden muss. Es ist sehr unwahrscheinlich, dass ein Sterilisator den Vakuumhaltetest besteht, den Test mit Versuchsladung jedoch nicht. Dennoch wurde dieser Fall bereits beobachtet. Diese Anomalie kann durch unzureichende Entlüftung während der Vorvakuumphasen und/oder durch mangelhafte Dampfqualität (Übermaß an nicht kondensierbaren Gasen, überhitzter Dampf oder feuchter Dampf) verursacht werden. Diese Tests sind temperatursensibel und für eine Temperatur von 132 °C (270 °F) ausgelegte Tests werden mit 121 °C (250 °F) ausgeführten Testzyklen nicht ordnungsgemäß ablaufen.
(Abbildung 6)
Die zehn häufigsten Fehler bei der Dampfsterilisation
Die häufigsten Fehler in Bezug auf Programmierung und Betrieb typischer Dampfsterilisatoren sind im Zusammenhang mit den Grundprinzipien der Dampfsterilisation zu sehen.
1. In den Sterilisator werden Container mit geschlossenen Ventilen, leere Glasflaschen mit fest verschlossenen Schraubverschlüssen oder fixierter Alufolie platziert.
In der Folge können die innenliegenden Oberflächen nicht direkt vom Dampf benetzt werden und es erfolgt keine Sterilisation. Dieses Problem lässt sich beheben, indem sichergestellt wird, dass sämtliches Sterilisiergut im Sterilisator einen Dampfeinlass und einen Luftauslass bietet. Wenn Unklarheiten bezüglich der für einen angemessenen Dampfdurchlass geeigneten Anordnung, Aufbau, Verpackung oder Ausrichtung des Sterilisierguts auftreten, lassen sich eindeutige Antworten mithilfe im Sterilisiergut eingeführter Thermoelemente, chemischer und/oder biologischer Indikatoren ermitteln.
2. In Beutel verpacktes und/oder massiv verpacktes Sterilisiergut wird eng zueinander in der Kammer platziert.
Folglich bleibt nach der Vorkonditionierungsphase Luft im Sterilisiergut eingeschlossen und verhindert die Sterilisation. Das Sterilisiergut darf nicht übermäßig verpackt sein und zwischen den Einzelteilen muss genügend Platz bleiben. Die Vakuum- und Druckpulse der Vorkonditionierung müssen ordnungsgemäß eingestellt sein, um eine vollständige Entlüftung des Sterilisierguts zu erzielen. In der Regel müssen mindestens vier Vorkonditionierungs-Vakuumpulse für ein Hg-Vakuum von mind. 711 mm (6,9 kPa (absolut)) programmiert werden, um auch im ungünstigsten Ladungszustand eine ausreichende Entlüftung zu gewährleisten. Für sehr kompakt angeordnetes Gut ist auf maximalem Vakuumniveau der Vorkonditionierung ggf. eine kurze (2 bis 5 min) Haltedauer notwendig, um genügend Zeit zur Entlüftung von eingeschlossener Luft einzuräumen. Die Druckpulse der Vorkonditionierung müssen für 21 bis 34,5 kPa (Messwerte) programmiert werden. Ein höherer Druck für die Vorvakuum-Druckpulse erzeugt ggf. eine übermäßige Überhitzung und verursacht damit Probleme bei der Temperaturstabilisierung während der ersten Minuten der Einwirkphase.
3. Schwerere Teile werden in den oberen Einschub gelegt.
Nach abgeschlossenem Sterilisationszyklus sind an der Außenseite der Verpackung des in den mittleren bis unteren Einschüben platzierten Guts Wassertröpfchen und/oder Flecken. Die Teile sind nicht trocken und können daher nicht aseptisch aus dem Sterilisator entnommen werden. Kondensation ist der natürliche Vorgang, bei dem Dampf mit kühleren Oberflächen der Ladung in Berührung kommt. Das Kondensat wird dabei durch die einzelnen Einschübe tropfen. Je dichter die Teile des Sterilisierguts aneinander liegen, desto mehr Kondensat entsteht. Daher müssen schwerere Elemente in den unteren Einschub gelegt werden. Zusätzlich sollte vor der Beladung mit dem Sterilisiergut in jeden Beladewagen des Sterilisators ein Baumwolltuch oder fusselfreies Handtuch gelegt werden, das das Kondensat absorbiert. Damit wird auch die Trocknung verbessert. Die Kondensationsoberfläche wird durch die Einlagen erheblich vergrößert und das Kondensat kann in der Trockenphase im Vergleich zur selben Kondensatmenge in Tröpfchen oder einer Wasseransammlung wesentlich schneller verdampfen.
4. Zu dichte Beladung oder unkorrekt angeordnetes Sterilisiergut.
In der Folge liegt nach abgeschlossenem Zyklus nasses oder feuchtes Sterilgut vor. Verpackte Elemente, die derart positioniert sind, dass sich Kondensflüssigkeit darin sammelt, können nicht getrocknet werden. Darum sollten die Elemente so gelegt werden, dass die Kondensflüssigkeit abfließen kann. Elemente (Verpackungen, Beutel, Filter oder andere poröse biologische Barrieren), die nach Abschluss des Zyklus noch nass sind, können bei Entnahme aus dem Sterilisator eine Kontaminierung des Sterilisierguts nicht ausschließen. Die Abkühlung des Sterilguts erfolgt außerhalb des Sterilisators, wodurch in der Verpackung eingeschlossenes Wasser in das verpackte Element eindringt. Somit kann jegliche in der Umgebung vorhandene Kontaminierung mit dem Wasser die sterile Barriere überwinden. Für nasses Sterilgut gibt es vielfältige weitere Ursachen. Die häufigsten Ursachen sind:
a. Ungenügend programmiertes Trockenvakuum oder Trocknungszeit
b. Gummi- und Plastikteile in Beutel (z. B. Gummistopper, Plastikschläuche) benötigen eine zusätzliche Trocknung (für diese Teile ist ein Prozess mit gepulster Luft- oder erwärmter gepulster Lufttrocknung erforderlich)
c. Nassdampf : Zur Beseitigung der am Sterilgut angesammelten Nässe gibt es keine einheitliche Lösung. Doch durch Experimentieren mit der Trocknungszeit, der Neuanordnung des Sterilisierguts, Reduzierung der Beladungsdichte, Modifizierung der Zykluseinstellungen und Untersuchung der Dampfqualität wird sich eine Lösung des Problems finden.
5. Beutel werden flach in die Einschübe des Sterilisators oder übereinander gelegt.
Dadurch weisen Beutel an der Innenseite Wassertröpfchen auf und können nicht aseptisch aus dem Sterilisator entnommen werden. Als typische Ursache ist zu sehen, dass beim Eindringen des Dampfes in den Beutel auf natürliche Weise Kondensflüssigkeit entsteht und dabei die Oberfläche des darin liegenden Sterilisierguts benetzt. Dieses Kondensat kann während der Trocknungsphase der Nachkonditionierung nicht entfernt werden. Daher müssen Beutel in angemessenen Abständen und in einem Ladegestell so positioniert werden, dass die Beutel nur auf der Kante aufliegen (Abb. 7), um eine Ansammlung von Kondensat im Beutel zu verhindern. Beutel dürfen nicht flach auf den Sterilisatoreinschub gelegt werden. Beutel dürfen nicht übermäßig bestückt werden. Berücksichtigen Sie, dass durch eine höhere Masse auch mehr Kondensflüssigkeit entsteht.
Um eine vollständige Verdampfung des Kondensats zu ermöglichen, muss ein ausreichendes Trocknungsvakuum und entsprechendeTrocknungszeit programmiert werden. Nassdampf muss vermieden werden. Für doppelte Beutelverpackungen sind ggf. zusätzliche Vorvakuumpulse mit einer Verweildauer bei maximalem Vakuumniveau und verlängerter Trocknungszeit erforderlich. Doppelte Verpackungen sollten in keinem Fall so angeordnet sein, dass die darin enthaltenen Elemente nicht sichtbar sind. Die Laschen der Beutel dürfen nicht übergeschlagen werden.
6. Flüssigkeit in belüfteten Containern sammelt sich in einem Auffanggefäß für übergekochte Flüssigkeiten (langsamer Entlüftungszyklus).
Das Auffanggefäß enthält Wasser und schließt damit enthaltene Luft ein. Die Oberfläche des Gefäßes ist dadurch vom Dampfkontakt aufgrund der eingeschlossenen Luft abgeschirmt und wird somit nicht sterilisiert. Zur Behebung des Problems sollte das Auffanggefäß entfernt und die langsame Entlüftungsrate im Sterilisator angepasst werden, um ein Überkochen zu verhindern. Für den Fall, dass sich eine geringe Menge von übergekochter Flüssigkeit durch Anpassung der langsamen Entlüftungsrate nicht vermeiden lässt, kann ein flaches Auffanggefäß, das maximal 25 mm tief ist, verwendet werden.
7. „Verkochte“ Medien.
Eine übermäßige Sterilisation der Medien karamelisiert die Zucker und macht die Medien nutzlos. Der typische Ansatz „Viel hilft viel“ ist für die Sterilisation von Medien nicht zu empfehlen. Die Einwirkphase sollte so programmiert werden, dass die gewünschte SAL erreicht wird, aber nicht länger. Die Verwendung einer Chargensonde und der Einwirkkontrolle F0 wird für die Sterilisation von Medien in Behältern über 100 ml empfohlen. Wie Abbildung 8 zeigt, ist F0 eine Funktion der äquivalenten Einwirkung bei anderen Temperaturen als 121,1 °C (250 °F). Wird die Flüssigkeit erhitzt, erhöht sich die berechnete F0 (von der Chargensondentemperatur), bis der gewählte F0-Einwirkwert (Minuten) erreicht wird. An diesem Punkt wechselt der Zyklus in die Entlüftungs-/Abkühlungsphase. Aus der Kurve erkennen wir zum Beispiel, dass die Keimabtötungsrate bei der gleichen Organismuspopulation bei 118 °C (245 °F) halb so effektiv ist wie bei 121 °C (250 °F). Daher muss die Einwirkzeit bei 118 °C (245 °F) zweimal so lang sein, um die gleiche Anzahl von Organismen zu töten.
(Abbildung 8)
Eine übliche Formel für die Berechnung von F0 ist:
![]()
Hierbei gilt:
• L ist Abtötungsrate bakterieller Sporen
• t ist die Einwirkzeit [s]
• T ist die Einwirktemperatur [ºC]
• z ist eine Konstante [ºC]
Die Konstante z beschreibt die Steigung der thermischen Abtötungskurve. Ein allgemein anerkannter Wert für z ist 10 ºC (18 ºF) bei der Dampfsterilisation.
8. Verwendung von kaltem Wasser bei einer zu heißen Vakuumpumpe.
Das kann dazu führen, dass die Vakuumpumpe 6,9 kPa nicht erreichen kann. Die Wasserringvakuumpumpe ist das Herz des Vorvakuum-Sterilisators. Die Effizienz und die maximale Vakuumleistung einer Wasserringvakuumpumpe werden durch höhere Wassertemperaturen, wie sie normalerweise in den Sommermonaten anzutreffen sind, beeinträchtigt. Während des Betriebs wird das Wasser in der Pumpe durch mechanische Reibung und die Wärmeenergie aus der Sterilisatorkammer aufgeheizt. Erreicht die Wassertemperatur in der Pumpe während der Vorkonditionierungs- oder Nachkonditionierungsvakuumspitze 39 °C (102 °F), siedet das Wasser in der Pumpe bei ≤ 6,9 kPa und verursacht Kavitation. In diesem Fall kann der empfohlene Vorkonditionierungsvakuumpegel von 6,9 kPa in der Sterilisatorkammer nicht erreicht werden. Als übliche Abhilfe für diese Situation wird der Sollwert der Vorvakuumimpulse auf einen erreichbaren Wert gesetzt. Daraus kann sich unzureichende Luftabsaugung ergeben, wenn die Anzahl der Vakuumimpulse nicht erhöht wird, was zu längeren Zykluszeiten und weniger effektiver Luftabsaugung führt. Interne Pumpentemperaturen von über 39 °C (102 °F) werden häufig während der Sommermonate beobachtet, wenn das an die Pumpe gelieferte Wasser nicht gekühlt wird. Gekühltes Wasser ist ideal, aber normalerweise zu teuer für die Verwendung in einer Sterilisator-Vakuumpumpenanordnung, in der das Wasser von der Vakuumpumpe in den Abfluss fließt. Die empfohlene Lösung ist ein Umwälz-/Kühlsystem für das Vakuumpumpenwasser, das gekühltes Wasser in einem geschlossenen Wärmetauscher verwendet. Diese Konfiguration ist umweltfreundlich und spart eine beträchtliche Menge Wasser. Zusätzlich unterliegt die Vakuumpumpeneffizienz keinen saisonalen Wassertemperaturschwankungen.
9. Chargensonde ist verfügbar, wird aber nicht verwendet.
Die meisten modernen Sterilisatoren schließen (optional) eine RTD-Chargensonde und eine F0-Einwirksteuerung für die Sterilisation in Flüssigkeiten ein, aber die Sonde wird häufig nicht verwendet. Ist eine Chargensonde vorhanden, kann die Einwirkung über die Temperatur der Flüssigkeit und nicht über die Temperatur in der Abflussleitung gesteuert werden. Ohne die Chargensonde ist die Temperatur der Flüssigkeit unbekannt und kann nur geschätzt werden, was zu einer unzureichenden (nicht steril) oder zu hohem F0 Wert(verkocht) führt. Die Chargensonde sollte in einen Wasserbehälter gesetzt werden, dessen Volumen etwa dem größten Volumen der zu sterilisierenden Flüssigkeit entspricht. In den Steuerungseinstellungen des Sterilisators muss dann die Chargensondensteuerung/F0 ausgewählt werden.
10. Druck-/Vakuumverhältnissteuerung ist verfügbar, wird aber nicht verwendet.
Die meisten modernen Sterilisatoren schließen (optional) eine Verhältnissteuerung für die Vakuum- und Druckanstiege ein, aber die Verhältnissteuerung wird häufig nicht verwendet. Wird keine Druckverhältnissteuerung verwendet, tritt während der Druckimpulse der Vorkonditionierung Dampf mit der maximalen Geschwindigkeit in die Kammer ein, was zu einem Überhitzungsproblem und den bereits diskutierten Verletzungen der Norm EN 285 führt. Die Verlangsamung des Druckanstiegs liefert Zeit für die Verteilung der Überhitzung während des Anstiegs.
Wird keine Vakuumverhältnissteuerung angewendet, fällt der Druck in der Kammer mit der Höchstgeschwindigkeit der Vakuumpumpe. Das damit normalerweise verbundene Problem sind zerplatzte Beutel. Die Verlangsamung des Druckabfalls liefert Zeit für den Ausgleich des Innendrucks und verhindert ein zerplatzen der Beutel während der Vorkonditionierungs- und Nachkonditionierungsvakuumphasen.
Schlussbemerkung
Die Dampfsterilisation ist ein Prozess, der von Grundprinzipien abhängt, die dem Sterilisator Nutzer manchmal unbekannt sind oder von ihm ignoriert werden. Ein großer Prozentsatz von Misserfolgen bei der Dampfsterilisation kann durch logische und praktische Anwendung dieser Grundprinzipien behoben werden. Es sollte beachtet werden, dass die sachgemäße Ausbildung der Sterilisator Nutzer diese Prinzipien einschließen sollte. Sachgemäße Verpackungs- und Beladungsverfahren sind für die sichere und erfolgreiche Sterilisation entscheidend. Wie bei allen kritischen Prozessgeräten ist eine sachgemäße Wartung und Eichung wesentlich.
Literaturangaben:
1. USP 35 , Biological Indicators for Sterilization, Table 1.
2. Lewis, R.G., "Practical Guide to Autoclave Validation, Pharmaceutical Engineering, July/August 2002 for further discussion of SAL.
3. Principles and Methods of Sterilization in Health Sciences, John J . Perkins, M.S. LL.D., F.R.S.H, Second Edition, Eighth Printing, 1983, Chapter 6, p. 137.
4. http://www.engineeringtoolbox.com/saturated-steamproperties-d_101.html.
5. The European Standard EN28S: Sterilization – Steam Sterilizers - Large sterilizers: 2006 + A2:2009; 8. Performance Requirements, 8.3.1.3, pp. 15-16.
6. Robert E. Beck; Autoclaving of Solutions in Sealed Containers: Theoretical Temperature – Pressure Relationship. Pharmaceutical Manufacturing Magazine, pages 18-23, June 1985
Über die Autoren
Marcel Dion ist Director of Marketing for Washing and Steam Sterilization Systems in der Life Sciences Division der Steris Corporation. Dion hat ein Diplom in Instrumentierung und Steuerung von Levis-Lauzon CEGEP in Quebec, Kanada. Während der ersten 20 Jahre seiner Karriere war er am Entwurf und der Herstellung von Waschsystemen für die pharmazeutische/biotechnologische Produktion involviert. In den vergangenen 13 Jahren war er verantwortlich für die Entwicklung und Markteinführung von innovativen und effizienten Reinigungs- und Dampfsterilisationssystemen für kritische Teile/Komponenten, die bei der Arzneimittelherstellung genutzt werden. Dion ist seit mehreren Jahren Mitglied der Organisationen ISPE, PDA, LAMA und AALAS. Er kann telefonisch kontaktiert werden: +1-418-664-7512. Steris, 490 Armand-Paris, Quebec G1C8A3, Kanada.
Wayne Parker ist ein unabhängiger Berater für die Sterilisation mit feuchter Hitze in der Pharmazie, Biotechnik und industriellen Forschung. Parker machte 1965 seinen Abschluss an der Hillsborough High School in Tampa, FL in 1965 als Mitglied der National Honor Society. Er besuchte die University of South Florida in Tampa von 1965 bis 1968. Parker diente von 1968 bis 1972 als Radar-Wartungsunteroffizier in der amerikanischen Luftwaffe und setzte seine Ausbildung an der U.S. Air Force Extension University fort. Als er „in Rente ging“, wurde er von 1972 bis 2012 von der American Sterilizer Co. (jetzt Steris Corporation) eingestellt. Während seiner Karriere hatte Parker zahlreiche Positionen inne, einschließlich Servicetechniker im Außendienst, cGMP-Spezialist im Außendienst, Bereichsverkaufsleiter und Großkundenbetreuer Pharmazie. Er führte Schulungen und Beratungsdienste bei zahlreichen Firmen durch und arbeitet weiterhin mehrere Male im Jahr als Gastdozent für Postgraduierte am College of Pharmacy der University of Tennessee in Memphis. Er ist seit mehreren Jahren Mitglied der Organisationen ISPE, PDA und AALAS. Er kann per E-Mail kontaktiert werden: autoclaveman2007@yahoo.com.
STERIS Deutschland GmbH
50933 Köln
Deutschland